Embriogenesi: perché studiare lo sviluppo embrionale umano
L’embriogenesi è la fase più delicata dello sviluppo umano, il momento in cui da una singola cellula uovo si origina un organismo complesso. Comprendere questi passaggi non è solo affascinante sul piano teorico, ma è anche indispensabile per interpretare numerose patologie congenite.
Dal punto di vista biologico, lo sviluppo embrionale integra in modo serrato genetica, biologia cellulare e fisiologia.
Ogni divisione cellulare, ogni migrazione, ogni segnale molecolare contribuisce alla costruzione di strutture sempre più specializzate. Per questo, nei corsi universitari di medicina e biologia, l’attenzione su queste fasi è in costante crescita.
Clinici e ricercatori utilizzano i modelli di embriogenesi per spiegare l’origine di difetti anatomici e funzionali, collegando le anomalie visibili alla nascita agli eventi precoci dello sviluppo.
Conoscere l’embriogenesi permette anche di leggere con maggiore accuratezza le immagini della diagnostica prenatale.
Le ecografie delle prime settimane, ad esempio, acquistano significato solo se messe in relazione con le tappe dello sviluppo. Questo articolo ripercorre cosa succede nelle diverse fasi: dalla fecondazione, alla formazione dei foglietti embrionali, fino all’abbozzo dei principali organi. Verranno presentati esempi concreti, con terminologia precisa ma spiegata in modo accessibile, così che anche uno studente universitario alle prime armi possa orientarsi con sicurezza.
Embriogenesi: fecondazione e formazione dello zigote
La prima tappa dell’embriogenesi è la fecondazione, un incontro estremamente regolato tra gameti maschili e femminili che avviene nelle tube uterine.
Questo evento segna l’inizio dello sviluppo individuale, perché determina una ricombinazione unica del patrimonio genetico.
Durante la fecondazione, uno spermatozoo attraversa gli involucri esterni della cellula uovo e ne fonde la membrana plasmatica.
La formazione del pronucleo maschile e femminile consente l’unione dei genomi parentali, dando origine al genoma diploide.
Il risultato è lo zigote, prima cellula dell’organismo, metabolicamente attiva e pronta ad avviare le divisioni mitotiche.
In una gravidanza tipica, la fecondazione avviene circa 14 giorni dopo l’inizio del ciclo mestruale.
Lo zigote inizia a dividersi già nelle prime 24 ore, mentre si sposta lungo la tuba verso la cavità uterina.
In questa fase, errori nei meccanismi di fusione tra gameti possono generare anomalie cromosomiche numeriche, come le trisomie, che spesso determinano un arresto molto precoce dello sviluppo.
Quando invece i processi procedono correttamente, lo zigote attiva un programma di divisioni cellulari rapide ma accuratamente coordinate.
Queste divisioni forniscono la base quantitativa dell’embriogenesi successiva e preparano il passaggio alla segmentazione, mantenendo al contempo l’integrità dell’informazione genetica e la capacità dell’embrione di adattarsi all’ambiente uterino iniziale.
Embriogenesi: segmentazione e compattazione embrione precoce
Con l’avvio delle prime divisioni mitotiche, l’embriogenesi entra nella fase di segmentazione, in cui lo zigote si suddivide in cellule progressivamente più piccole, chiamate blastomeri.
In questo periodo il volume globale dell’embrione non aumenta in modo significativo, ma cambia la distribuzione e l’organizzazione delle cellule.
Tra il primo e il terzo giorno dopo la fecondazione, il numero di cellule raddoppia a ritmo serrato.
L’embrione passa da 2 a 4, poi a 8 e infine a 16 blastomeri. Intorno allo stadio a 16–32 cellule, i blastomeri iniziano ad aderire strettamente gli uni agli altri: è la compattazione, che conduce alla formazione dello stadio morula.
In ambito clinico, durante le procedure di fecondazione in vitro, l’embrione viene spesso valutato proprio in questa fase. Si osservano la simmetria, la dimensione dei blastomeri e il grado di compattazione, parametri utili per stimare il potenziale di sviluppo.
La compattazione modifica le giunzioni intercellulari e crea una netta polarità tra cellule esterne e interne.
Le cellule esterne contribuiranno alle strutture di sostegno, mentre quelle interne costituiranno la massa cellulare embrionale vera e propria. Questo passaggio indirizza il destino cellulare e assicura che l’embriogenesi proceda verso strutture più complesse, preservando la coesione del gruppo cellulare in crescita.
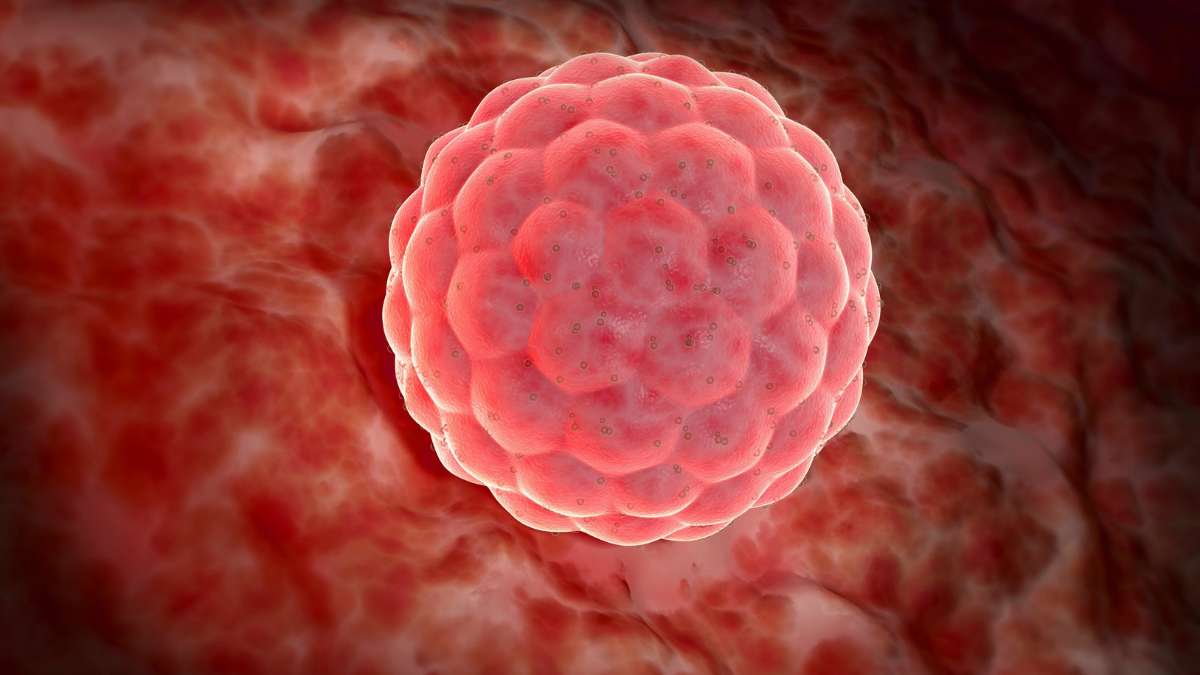
Formazione della blastocisti e impianto nell’utero
La fase successiva dell’embriogenesi è la formazione della blastocisti, una struttura cava fondamentale per instaurare il dialogo con l’endometrio materno.
In questo stadio, l’embrione acquisisce una chiara organizzazione spaziale che prepara l’interazione con l’utero.
All’interno della morula si forma una cavità piena di liquido, la blastocele.
Le cellule interne costituiscono la massa cellulare interna, destinata all’embrione vero e proprio, mentre quelle periferiche formano il trophoblasto, che darà origine a parte della placenta e alle membrane di sostegno.
Intorno al quinto giorno, la blastocisti rompe gli involucri che la circondano e si prepara all’impianto nella mucosa uterina.
Per visualizzare meglio questa fase, è utile ricordare alcuni elementi fondamentali:
- Ruolo del trophoblasto nell’adesione all’endometrio
- Comunicazione chimica tra embrione e tessuto materno
- Modificazioni vascolari locali nella mucosa uterina
- Stabilizzazione ormonale necessaria al proseguimento della gravidanza
Un classico esempio clinico è l’impianto fuori sede, ovvero la gravidanza ectopica, in cui la blastocisti aderisce alle tube anziché all’utero.
In queste condizioni l’embriogenesi non può procedere in modo normale, a causa dell’ambiente anatomico e vascolare inadeguato. Questo quadro mette in evidenza quanto l’interazione corretta tra blastocisti ed endometrio sia determinante per lo sviluppo successivo.
Gastrulazione e organizzazione dei foglietti embrionali
Con la gastrulazione, l’embriogenesi entra in una fase qualitativamente nuova, durante la quale si definiscono i foglietti germinativi fondamentali.
L’embrione passa da una struttura prevalentemente bidimensionale a un’architettura tridimensionale complessa, con piani corporei ben impostati.
Durante la gastrulazione, le cellule migrano in modo coordinato attraverso il nodo primitivo e la linea primitiva.
In questo modo si formano ectoderma, mesoderma ed endoderma, ciascuno con destini istologici e funzionali specifici.
L’ectoderma origina sistema nervoso centrale e periferico, oltre all’epidermide; il mesoderma genera muscoli, ossa e apparato cardiovascolare; l’endoderma forma l’epitelio intestinale e molte ghiandole associate.
Nei modelli sperimentali su mammiferi, anche minimi errori nelle traiettorie di migrazione del mesoderma determinano difetti cardiaci strutturali, rilevabili già nelle prime ecografie.
Questo collegamento diretto tra dinamica cellulare e anatomia finale rende la gastrulazione una fase chiave per comprendere l’origine delle malformazioni.
Questa fase dell’embriogenesi è essenziale anche per l’impostazione degli assi corporei.
Gradienti di fattori di crescita e reti di geni regolatori definiscono le regioni craniale e caudale, dorsale e ventrale.
Saper interpretare correttamente la gastrulazione permette di collegare la posizione di un organo adulto al suo foglietto embrionale d’origine, chiarendo la base di molte varianti anatomiche e di numerosi quadri clinici.
Neurulazione, assi corporei e primi abbozzi di organi
Dopo la gastrulazione, l’embriogenesi prosegue con la neurulazione, cioè la formazione del sistema nervoso primitivo.
Da una regione specializzata dell’ectoderma si sviluppa la placca neurale, che si ripiega progressivamente fino a chiudersi e a formare il tubo neurale.
Durante la neurulazione, la chiusura del tubo neurale avanza lungo l’asse cranio-caudale secondo una sequenza precisa.
Difetti in questo processo portano a malformazioni come spina bifida e anencefalia, condizioni che la diagnostica prenatale può individuare relativamente presto.
Nello stesso intervallo temporale, il mesoderma para-assiale dà origine ai somiti, precursori segmentali di vertebre, muscoli scheletrici e parte del derma.
Intorno alla quarta settimana, un embrione umano presenta già diverse coppie di somiti visibili in microscopia, segno di una segmentazione corporea avanzata.
In parallelo, l’endoderma inizia a modellare il tubo intestinale primitivo, che costituirà la base per lo sviluppo di organi come lo stomaco e l’intestino, segnando l’avvio dell’organogenesi.
In questa fase, l’embriogenesi integra segnali meccanici, chimici ed elettrici.
Gradienti di molecole come la sonic hedgehog (Shh) indirizzano la differenziazione cellulare in molte regioni dell’embrione. Comprendere questi equilibri consente di interpretare le basi cellulari di numerose malformazioni congenite identificate in epoca prenatale.
Studi recenti mostrano come l’interazione tra tali segnali influenzi non solo lo sviluppo del sistema nervoso, ma anche la formazione di strutture vitali come cuore e reni, evidenziando il ruolo cruciale di un ambiente uterino adeguato per uno sviluppo embrionale sano.
L’embriogenesi come chiave interpretativa della biologia umana
L’embriogenesi offre una lente privilegiata per comprendere come sequenze estremamente precise di eventi generino una complessità biologica ordinata. Dalla fecondazione alla neurulazione, ogni passaggio organizza spazio, tempo e informazione genetica con rigore sorprendente.
Per la biomedicina moderna, questa conoscenza ha implicazioni concrete.
Lo studio dei meccanismi che guidano l’embriogenesi sostiene la ricerca sulle malformazioni congenite, orienta la diagnostica prenatale e chiarisce le basi cellulari di terapie innovative.
La scoperta delle cellule staminali embrionali ha aperto alla rigenerazione tissutale e alla medicina rigenerativa, mostrando come una comprensione approfondita dell’embriogenesi possa tradursi in applicazioni cliniche rivoluzionarie.
Osservare le fasi dello sviluppo significa anche confrontarsi con il potenziale racchiuso in una singola cellula e con i limiti di ogni sistema biologico.
La precisione richiesta per completare correttamente queste tappe rivela quanto sia sottile l’equilibrio tra normalità e patologia.
La possibilità di intervenire molto precocemente su anomalie dello sviluppo, grazie a tecniche come l’editing genetico, evidenzia ulteriormente il valore di una conoscenza dettagliata di questi processi.