Legame ionico: contesto chimico e trasferimenti di carica
Capire come si forma un legame ionico sembra spesso un ostacolo insormontabile. In realtà rappresenta un passaggio decisivo per leggere davvero la chimica fisica.
Nei libri compaiono schemi semplificati, con palline colorate che si scambiano elettroni. Tuttavia dietro quelle immagini c’è una descrizione precisa del comportamento microscopico della materia. Comprendere questa descrizione richiede di collegare insieme concetti come teoria atomica, carica elettrica e struttura elettronica. Senza questo collegamento molti esercizi risultano meccanici e poco chiari.
Per uno studente di scuola superiore, la formazione del legame tra ioni è spesso il primo contatto serio con la chimica quantitativa.
Qui non basta ricordare definizioni: serve capire perché gli ioni si attraggono e perché alcune combinazioni sono più stabili di altre.
Questo tema ha implicazioni dirette su solubilità dei sali, conduzione elettrica delle soluzioni, acidità e pH.
Inoltre entra in molte domande d’esame, sia scritte sia orali.
In questa guida analizzerai passo passo la nascita di un legame tra ioni, dal punto di vista energetico e strutturale. Vedrai come la carica delle particelle, la distanza e la configurazione elettronica determinano la stabilità del composto. Infine collegherai questi concetti agli esercizi tipici, così la teoria non resterà scollegata dai calcoli.
Basi teoriche del legame ionico nell’atomo
Per capire davvero un legame ionico devi partire dalla struttura dell’atomo.
Ogni nucleo contiene protoni positivi e neutroni neutri, circondati da elettroni negativi.
La disposizione degli elettroni segue principi ben precisi, descritti dalla teoria atomica quantistica. Gli elettroni più esterni, detti di valenza, controllano le reazioni chimiche.
Un sistema è particolarmente stabile quando il livello più esterno è completo, come nei gas nobili. Per questo molti elementi tendono a perdere o acquistare elettroni, avvicinandosi a quelle configurazioni.
Quando un elemento perde elettroni forma un catione; quando li acquista forma un anione.
Questo processo di ionizzazione è associato a una certa energia di ionizzazione.
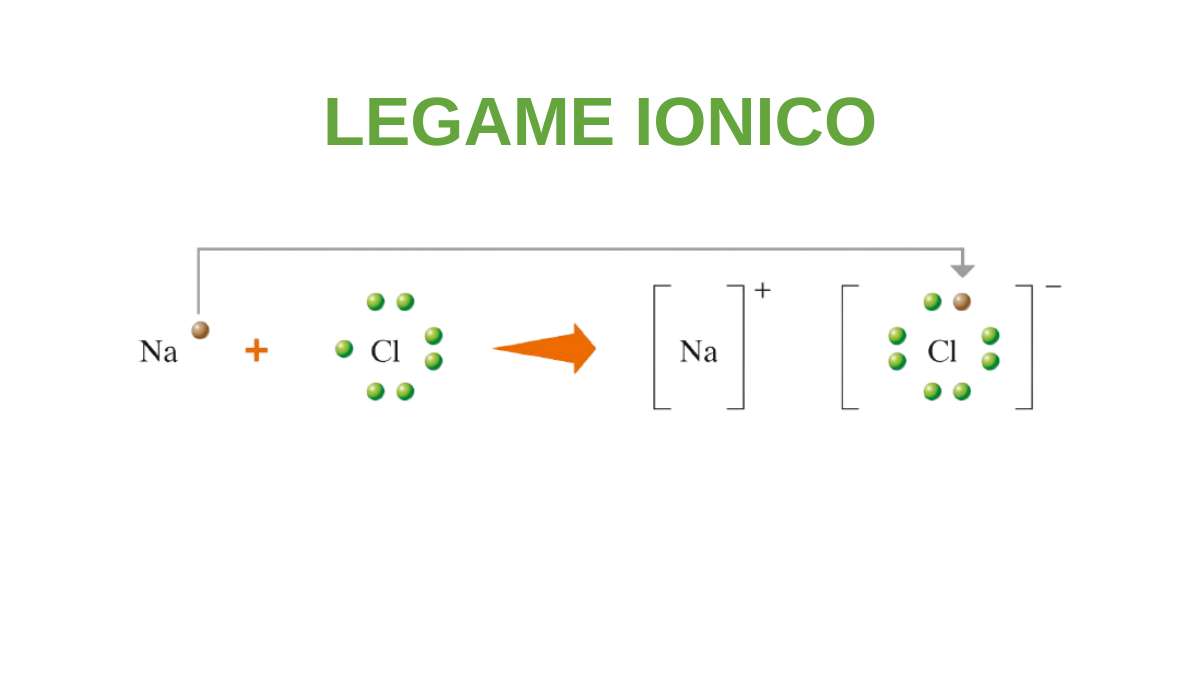
Se consideri il sodio neutro, possiede un elettrone di valenza relativamente poco legato. Cedendolo, diventa Na⁺ con configurazione simile al neon.
Il cloro, invece, ha quasi completo il livello esterno e tende ad acquistare un elettrone, diventando Cl⁻.
L’incontro tra Na⁺ e Cl⁻ porta alla formazione di cloruro di sodio, un classico esempio di legame ionico semplice da analizzare.
Questo schema, però, vale per moltissimi altri sali, con cariche e rapporti stechiometrici diversi. Comprendere bene queste trasformazioni ti permette di prevedere quali coppie di elementi formano un legame ionico e quali, invece, preferiscono un legame covalente o metallico.
Forze elettrostatiche e nascita del legame tra ioni
La formazione di un legame ionico non è un semplice “incastro” di sfere.
È il risultato di forze elettrostatiche che agiscono tra cariche opposte. La legge di Coulomb descrive questa interazione attraverso l’espressione \[F = k \frac{q_1 q_2}{r^2}\].
La forza aumenta con il valore assoluto delle cariche e diminuisce con il quadrato della distanza.
Quindi ioni con carica ±2 si attraggono più fortemente di ioni con carica ±1 alla stessa distanza. Questo dato spiega perché composti come MgO hanno punti di fusione più elevati del NaCl.
Quando un atomo metallico si ionizza, l’elettrone ceduto viene acquisito da un non metallo. Subito dopo, le cariche opposte si attraggono e si avvicinano, rilasciando energia.
La formazione del legame tra ioni è favorita se l’energia totale liberata supera quella spesa per ionizzare l’elemento donatore.
Nel caso del calcio che reagisce con il cloro, si formano Ca²⁺ e due ioni Cl⁻. Le attrazioni tra Ca²⁺ e ciascun anione contribuiscono alla stabilità di CaCl₂ solido.
In un cristallo reale ogni ione interagisce con molti vicini, non solo con un partner singolo. Per questo si introduce il concetto di energia reticolare, che misura l’energia necessaria per separare completamente il reticolo di ioni. Valori elevati indicano reticoli molto stabili e punti di fusione alti.
Fattori che favoriscono un legame ionico stabile
Non tutte le coppie di elementi formano con facilità un legame ionico.
La probabilità dipende da diversi fattori energetici e strutturali. Il primo è la differenza di elettronegatività tra i due elementi.
Se un elemento tende molto a perdere elettroni e l’altro a guadagnarli, il trasferimento risulta conveniente.
Contano anche il raggio ionico e la possibilità di impacchettare ordinatamente le cariche nel reticolo. Ecco i principali fattori che puoi tenere a mente durante lo studio:
- Grande differenza di elettronegatività tra catione e anione
- Bassa energia di ionizzazione dell’elemento che dona elettroni
- Elevata affinità elettronica dell’elemento che li riceve
- Possibilità di formare un reticolo cristallino compatto
Se metti a confronto sodio e cloro, trovi una grande differenza di elettronegatività.
Il sodio ha bassa energia di ionizzazione e cede facilmente un elettrone. Il cloro possiede elevata affinità elettronica e lo accetta volentieri.
Il risultato è la formazione di Na⁺ e Cl⁻ che si organizzano in un reticolo regolare, con elevata energia reticolare.
Al contrario, una coppia come idrogeno‑fluoro dà origine soprattutto a un legame covalente polarizzato, non a un classico legame ionico esteso.
In sistemi come MgO o CaO le cariche sono ±2 e il reticolo è ancora più compatto. Studiare questi esempi ti permette di collegare numeri tabulati, come raggi ionici ed energie, alla stabilità concreta dei composti solidi.
Struttura cristallina, proprietà fisiche e soluzioni ioniche
Nel solido, gli ioni legati da un legame ionico occupano posizioni regolari in una struttura cristallina tridimensionale.
Ogni catione è circondato da anioni e viceversa, in un pattern ripetitivo detto cella elementare.
La neutralità complessiva è garantita dal bilancio tra cariche positive e negative. Questa organizzazione porta a proprietà fisiche caratteristiche.
I sali hanno in genere punti di fusione e di ebollizione elevati, perché serve molta energia per spezzare le interazioni tra ioni. Inoltre risultano duri ma fragili: un piccolo spostamento dei piani ionici può far combaciare cariche uguali, causando repulsione e frattura del cristallo.
Quando un sale come NaCl si scioglie in acqua, il reticolo si disgrega e si formano ioni solvata. In soluzione acquosa il composto conduce corrente grazie al movimento di Na⁺ e Cl⁻.
In laboratorio descrivi queste soluzioni usando la molarità, ossia moli di soluto per litro. Molte proprietà delle soluzioni ioniche, come abbassamento crioscopico e innalzamento ebullioscopico, dipendono dal numero totale di particelle disciolte: sono le cosiddette proprietà colligative.
Anche il pH può variare: un sale derivato da un acido forte e una base debole produce soluzioni acide, mentre l’opposto genera soluzioni basiche.
Connettere legame ionico, concentrazioni e comportamento in soluzione ti aiuta a interpretare dati sperimentali con maggiore sicurezza.
Confronto tra legame ionico, covalente e metallico
Per non isolare il concetto di legame ionico conviene confrontarlo con altri tipi di legame.
Nel legame covalente due atomi condividono coppie di elettroni, invece di trasferirle.
Se la differenza di elettronegatività è piccola, il legame resta quasi omopolare, come in H₂.
Quando aumenta, si parla di legame covalente polare, perché la densità elettronica si concentra verso l’atomo più elettronegativo. Oltre un certo limite di differenza, risulta energeticamente preferibile il trasferimento completo dell’elettrone, tipico del legame tra ioni.
Nei metalli, infine, gli elettroni di valenza sono delocalizzati su tutto il reticolo, dando origine al legame metallico.
Molti processi che portano alla formazione di un legame ionico coincidono con vere reazioni redox.
L’atomo che perde elettroni si ossida, quello che li acquista si riduce. In celle galvaniche, la tendenza di una specie a ossidarsi o ridursi si descrive con potenziali standard e con l’equazione di Nernst.
In soluzione, gli ioni che hai ottenuto dal solido ionico partecipano a questi equilibri elettrochimici. Collegando il legame tra ioni alla variazione di numero di ossidazione puoi leggere gli schemi redox con maggiore coerenza. Questa visione unificata rende meno frammentari capitoli che spesso vengono studiati separatamente.
Una visione unitaria dei legami e della materia
Raggiungere una comprensione solida del legame ionico significa andare oltre gli schemi con frecce colorate.
Il quadro che emerge integra struttura dell’atomo, energia di ionizzazione, affinità elettronica, forze coulombiane e organizzazione del reticolo.
Ogni sale che incontri in laboratorio diventa così un caso concreto dove questi concetti si intrecciano. La stessa formula, come NaCl o MgO, racchiude già informazioni su carica degli ioni, stabilità termica, comportamento in soluzione e possibili reazioni redox.
Vista da questa prospettiva, la chimica di base non è più una raccolta di definizioni da memorizzare. Diventa una descrizione coerente di come la materia cerca configurazioni energeticamente favorevoli. Il legame ionico rappresenta uno dei meccanismi fondamentali attraverso cui questa ricerca si realizza.
Comprenderlo in profondità illumina anche i capitoli successivi, dalle soluzioni elettrolitiche alla chimica elettrochimica avanzata. La prossima volta che osserverai un cristallo di sale, potresti domandarti quante leggi fisiche, apparentemente astratte, si manifestano silenziosamente in quella semplice struttura.