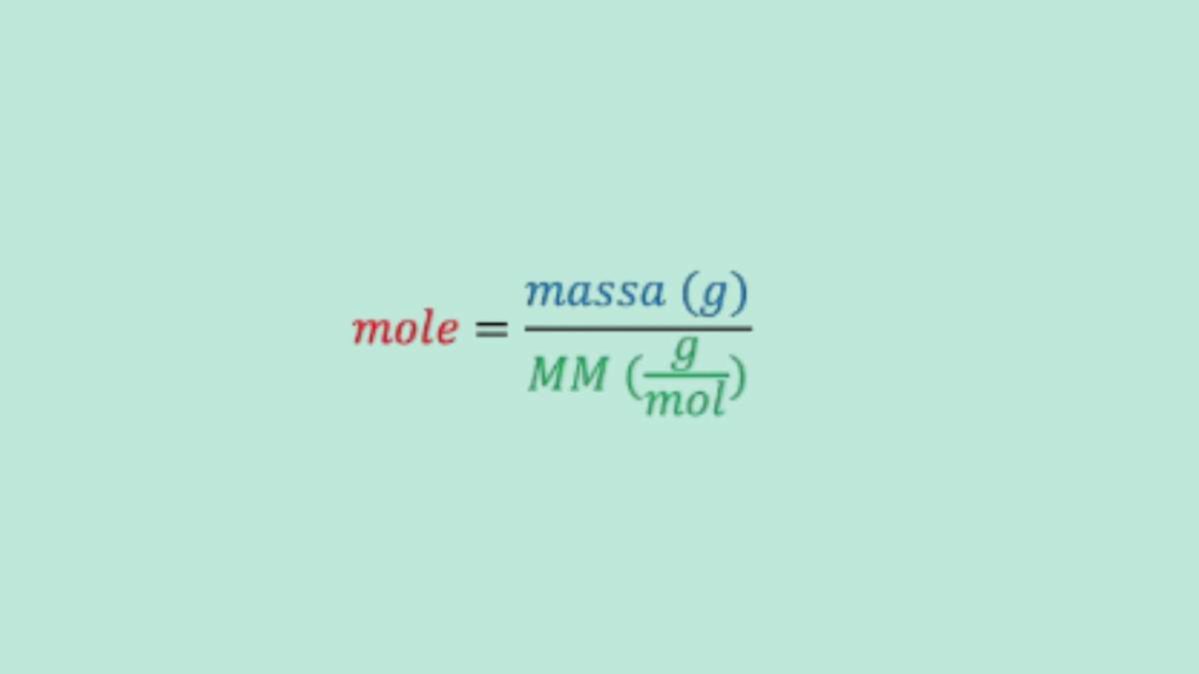Mole: comprendere la quantità di sostanza
La mole è la chiave che collega il mondo degli atomi con quello dei becher sul banco di laboratorio. Senza questo concetto, numeri e formule chimiche restano astratti e difficili da gestire.
In chimica la quantità di sostanza, indicata con n, è una grandezza fondamentale del Sistema Internazionale.
Serve per contare entità microscopiche, come atomi, ioni o molecole, usando un’unità pratica. Al centro c’è il numero di Avogadro, che indica quante particelle contiene una mole. Grazie a questo ponte concettuale possiamo tradurre una massa misurata sulla bilancia nel numero di particelle effettivamente presenti nel campione.
Capire bene cos’è la mole ha effetti immediati sul modo in cui imposti esercizi, reazioni e problemi di laboratorio. Riduce gli errori di ordine di grandezza e chiarisce i rapporti tra reagenti e prodotti. In questo articolo vedrai che la mole non è solo una definizione da ricordare, ma uno strumento operativo.
Analizzeremo la definizione formale, il legame con il numero di Avogadro, le conversioni tra massa, moli e particelle. Vedrai esempi di calcoli stechiometrici, errori tipici degli studenti e strategie per usare la mole in modo sicuro e rapido.
Definizione rigorosa di mole e ruolo del numero di Avogadro
In termini rigorosi, la mole è la quantità di sostanza che contiene un numero definito di entità elementari. Queste entità possono essere atomi, molecole, ioni o elettroni, a seconda del contesto del problema chimico.
Il numero esatto di entità contenute in una mole è il numero di Avogadro, indicato con \(N_A\).
Il suo valore è fissato per definizione a \(N_A = 6{,}022 \times 10^{23}\) entità per mole.
Questo significa che una mole di acqua contiene \(6{,}022 \times 10^{23}\) molecole di \(\ce{H2O}\), indipendentemente dalla massa complessiva del campione.
Il legame chiave tra quantità di sostanza \(n\) e numero di particelle \(N\) è espresso dalla relazione \(n = \frac{N}{N_A}\).
Se misuri un campione che contiene \(1{,}2044 \times 10^{24}\) molecole di \(\ce{CO2}\), puoi calcolare le moli presenti.
Dividi il numero di particelle per \(N_A\): ottieni circa 2,00 mol. Questo passaggio logico rende gestibile un numero di particelle enormemente grande, trasformandolo in una quantità di sostanza facile da usare nei calcoli.
Comprendere che la mole è un’unità di conteggio, paragonabile a “dozzina” ma con un valore molto maggiore, aiuta a visualizzare i processi chimici. Ogni volta che bilanci un’equazione, in realtà stai ragionando in moli e quindi in rapporti fra quantità di sostanza, non fra grammi.
Come convertire tra massa, moli e numero di particelle
Per usare in modo efficace la mole, devi saper passare con sicurezza tra massa, moli e particelle.
La relazione chiave coinvolge la massa molare, indicata con \(M\), espressa in \(\text{g mol}^{-1}\).
La formula operativa è \(n = \frac{m}{M}\).
Dove \(m\) è la massa in grammi.
Se hai 18,0 g di acqua, con massa molare circa 18,0 \(\text{g mol}^{-1}\), calcoli \(n = \frac{18{,}0}{18{,}0} = 1{,}00\) mol. Per ottenere il numero di particelle usi \(N = n \times N_A\). Nel caso dell’acqua, una mole corrisponde a \(6{,}022 \times 10^{23}\) molecole.
Considera un campione di 11,5 g di cloruro di sodio \(\ce{NaCl}\), con massa molare approssimativa 58,5 \(\text{g mol}^{-1}\). Dividendo \(11{,}5\) per \(58{,}5\) ottieni 0,196 mol.
Moltiplicando per \(N_A\) trovi il numero di unità formula presenti. In un esercizio d’esame, una gestione rapida di questi passaggi evita errori di fattore mille, molto comuni.
Collegare mentalmente massa, mole e numero di particelle ti permette di leggere subito il significato fisico dei dati forniti. Non lavori più con cifre astratte, ma vedi quante entità chimiche partecipano davvero alla trasformazione descritta dalla reazione.
Cosa rappresenta una mole per atomi, molecole, ioni e gas
La mole non cambia valore numerico, ma il tipo di entità che conta dipende dal contesto. Questo punto è essenziale per interpretare correttamente i problemi di chimica generale.
Per un elemento monoatomico come il sodio metallico, una mole corrisponde a \(6{,}022 \times 10^{23}\) atomi di \(\ce{Na}\).
Per una sostanza molecolare come l’ossigeno gassoso \(\ce{O2}\), una mole rappresenta \(6{,}022 \times 10^{23}\) molecole di \(\ce{O2}\), quindi il doppio di atomi di ossigeno.
Per un sale ionico come il solfato di sodio \(\ce{Na2SO4}\), una mole indica altrettante unità formula, cioè pacchetti minimi ripetuti nel cristallo.
Nel caso dei gas ideali, una mole occupa un volume caratteristico.
A condizioni standard, una mole di gas ideale occupa circa 22,4 L. Questo permette di passare direttamente tra moli e litri per gas come \(\ce{N2}\) o \(\ce{O2}\), usando la legge dei gas ideali \(PV = nRT\).
Se un esercizio indica 44,8 L di ossigeno a condizioni standard, puoi riconoscere immediatamente la presenza di 2,00 mol.
Capire cosa conta la mole in ogni situazione ti consente di impostare correttamente i rapporti stechiometrici. Leggi così le reazioni come rapporti di particelle, piuttosto che come semplici numeri davanti alle formule chimiche.
La mole nei calcoli stechiometrici: metodo e passaggi chiave
Nei calcoli stechiometrici, la mole è lo strumento centrale per collegare i reagenti ai prodotti. Ogni coefficiente stechiometrico in un’equazione bilanciata indica un rapporto tra moli, non tra grammi.
Considera la reazione di combustione del metano: \(\ce{CH4 + 2 O2 -> CO2 + 2 H2O}\).
I coefficienti indicano che una mole di \(\ce{CH4}\) reagisce con due moli di \(\ce{O2}\) per formare una mole di \(\ce{CO2}\) e due moli di \(\ce{H2O}\). Se disponi di 3,0 mol di metano, servono 6,0 mol di ossigeno perché la combustione avvenga in modo completo.
Da questi dati puoi ricavare le masse e i volumi necessari.
Ecco i principali elementi da seguire in un esercizio stechiometrico:
- Trasforma sempre masse o volumi in moli
- Usa i coefficienti dell’equazione per il rapporto tra moli
- Trova il reagente limitante, se necessario
- Riconverti le moli finali in grammi o litri
Se devi sapere quanti grammi di acqua si ottengono, parti dalle moli di metano e usi i coefficienti. Con 3,0 mol di \(\ce{CH4}\) si formano 6,0 mol di \(\ce{H2O}\).
Moltiplicando per la massa molare dell’acqua ottieni la massa di prodotto. Questo approccio, sempre basato sulla quantità di sostanza, rende sistematici anche gli esercizi più lunghi.
Errori tipici sul concetto di mole
Molti errori nascono da una visione confusa di cosa rappresenti davvero la mole. Riconoscere questi punti deboli aiuta a prevenirli durante lo studio e durante le prove.
Un errore classico consiste nel trattare i coefficienti stechiometrici come rapporti tra grammi invece che tra moli.
Questo porta a risposte numeriche apparentemente plausibili ma concettualmente sbagliate.
Un altro fraintendimento frequente riguarda il volume molare dei gas: alcuni studenti lo usano a qualsiasi condizione, dimenticando che circa 22,4 L per mole valgono solo a condizioni standard.
C’è poi la confusione tra massa molare e massa atomica relativa, che ha lo stesso valore numerico ma unità diverse.
Un ulteriore problema nasce quando si dimentica il legame tra mole e numero di Avogadro.
Senza questo collegamento, il passaggio da moli a particelle viene gestito in modo meccanico, con rischio di errori di esponente. Chiarire sempre quali grandezze stai usando, e controllare le unità, rende i calcoli sulla quantità di sostanza più controllabili e coerenti.
Guardare la chimica attraverso il prisma della mole
Governare il concetto di mole significa cambiare prospettiva sulla chimica, dal semplice esercizio numerico alla lettura strutturata dei processi.
Ogni reazione diventa una storia ordinata di particelle che si incontrano in proporzioni precise, rese misurabili grazie alla quantità di sostanza.
Il numero di Avogadro smette di essere un valore da memorizzare e diventa la scala con cui misuri l’invisibile.
Le formule come \(n = \frac{m}{M}\) o \(N = n \times N_A\) non sono più simboli astratti, ma strumenti per collegare la bilancia, il cilindro graduato e il mondo microscopico.
Quando la mole è chiara, anche concetti più avanzati, come la cinetica o l’equilibrio chimico, risultano meno opachi.
Vedi sempre dietro ogni concentrazione, ogni coefficiente stechiometrico, un certo numero di entità che interagiscono.
In questa visione, la quantità di sostanza non è solo una grandezza del Sistema Internazionale. È il linguaggio minimo con cui la chimica descrive la realtà materiale, dal laboratorio scolastico alle applicazioni industriali più sofisticate.