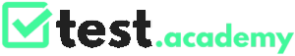Numero atomico: fondamenti degli elementi chimici
Capire il numero atomico significa leggere la struttura profonda della materia con uno sguardo davvero consapevole. Senza questo concetto, la chimica moderna resterebbe solo un elenco di fatti scollegati.
Ogni elemento possiede una identità ben precisa, legata ai suoi protoni e alla distribuzione degli elettroni. Il numero atomico formalizza proprio questa identità, offrendo un criterio rigoroso per distinguere un elemento dall’altro.
Per questo la teoria atomica lo pone al centro della descrizione microscopica della materia, dalle sostanze più semplici ai materiali complessi. Conoscere questo valore non serve solo negli esercizi: permette di prevedere proprietà, reattività e perfino il comportamento in condizioni estreme.
Questo tema conta molto anche per chi studia altre grandezze, come massa atomica e massa molecolare, o affronta argomenti avanzati come gli isotopi e le reazioni nucleari.
Comprendere davvero il numero atomico consente infatti di collegare concetti apparentemente lontani in un unico quadro coerente.
Di seguito vedrai cosa indica esattamente, come si misura, perché organizza la tavola degli elementi e in che modo entra nel calcolo di processi chimici e fisici rilevanti, dalle reazioni di laboratorio alle tecnologie mediche.
Definizione rigorosa di numero atomico
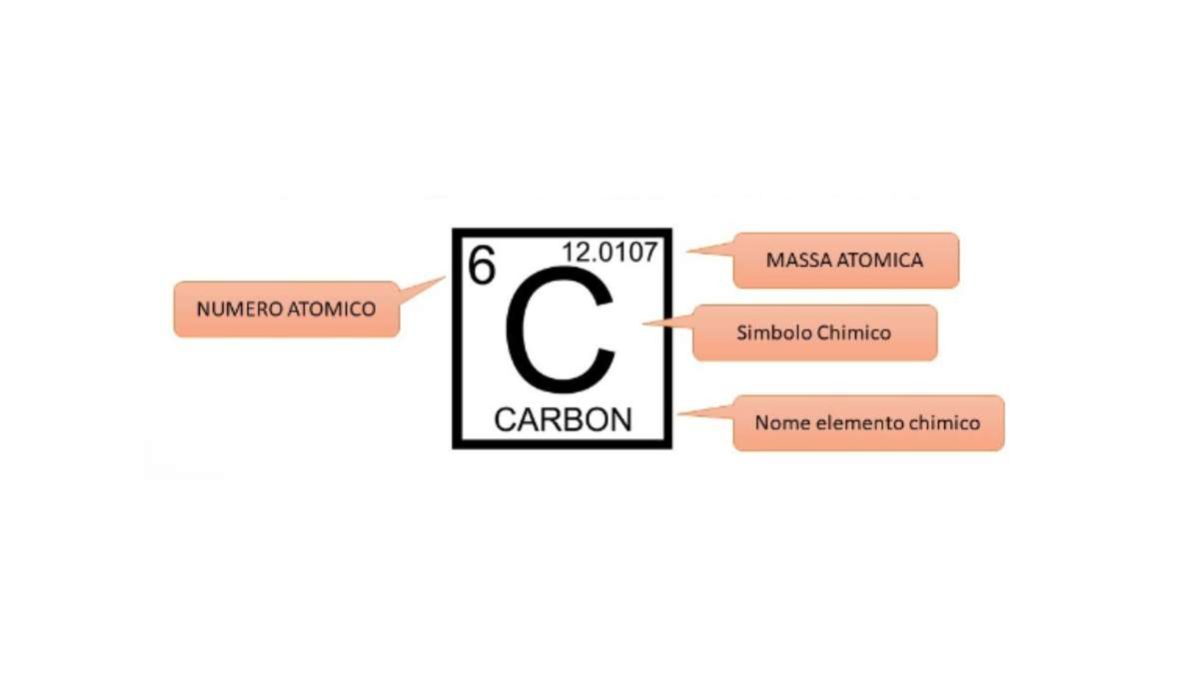
In chimica, il numero atomico indica il conteggio dei protoni presenti nel nucleo di un atomo. Ogni specie elementare possiede un valore univoco, indicato con la lettera Z nei testi scientifici.
Dal punto di vista sperimentale, questo numero deriva da misure di carica nucleare, inizialmente ottenute con tecniche di spettroscopia e diffrazione.
Conoscere Z permette di distinguere elementi che possono avere massa simile ma comportamento completamente diverso.
Un nucleo con 6 protoni identifica sempre il carbonio, mentre con 8 protoni indicherai l’ossigeno, indipendentemente dalla massa complessiva. Questo rende il numero atomico un parametro più fondamentale della massa stessa per la classificazione degli elementi.
Nei corsi di Fondamenti della teoria atomica, Z compare fin dalle prime lezioni, perché collega struttura interna e proprietà macroscopiche.
Il numero atomico stabilisce anche il numero di elettroni di un atomo neutro, condizionando configurazione elettronica e reattività chimica.
Dal punto di vista operativo, sapere leggere e interpretare Z accelera molti ragionamenti: riconosci subito analogie tra elementi, prevedi i tipi di legame possibili e interpreti tabelle di dati con maggiore sicurezza, evitando di affidarti solo alla memoria mnemonica.
Relazione tra numero atomico, massa e isotopi
Quando analizzi un elemento, numero atomico e massa non raccontano la stessa storia. Z fissa i protoni, mentre la massa dipende anche dai neutroni presenti nel nucleo.
Gli isotopi sono specie con lo stesso numero atomico ma diverso numero di neutroni.
Per esempio, il carbonio con Z = 6 possiede almeno due isotopi stabili importanti: C-12 e C-13.
Entrambi hanno 6 protoni, quindi mantengono lo stesso comportamento chimico di base. Tuttavia differiscono leggermente in massa, con effetti misurabili in spettrometria e nelle reazioni nucleari.
Qui il numero atomico resta invariato, mentre la massa atomica media cambia secondo l’abbondanza relativa.
Quando studi la massa molecolare, tieni conto della media pesata degli isotopi di ciascun elemento.
Il numero atomico determina le interazioni elettroniche, dunque la struttura dei legami; la massa condiziona invece fenomeni come diffusione, vibrazioni molecolari e stabilità di alcuni composti. Se distingui nettamente i ruoli di Z e della massa, interpreti meglio dati sperimentali complessi.
Inoltre, questa distinzione chiarisce perché la stessa formula chimica, ma con isotopi diversi, può mostrare comportamenti differenti in contesti biologici, ambientali o industriali.
Numero atomico e struttura elettronica dell’atomo
Il numero atomico stabilisce quanti elettroni possiede un atomo neutro, quindi controlla direttamente la sua struttura elettronica. Da qui discendono gran parte delle proprietà chimiche osservabili.
La disposizione degli elettroni nei vari livelli energetici segue regole definite, come il principio di Aufbau e il principio di esclusione di Pauli.
Con Z basso, gli elettroni occupano pochi livelli; aumentando il numero atomico, popolano orbitali sempre più esterni e complessi. Questo influenza raggio atomico, energia di ionizzazione e affinità elettronica.
Per esempio, l’elio con Z = 2 possiede un guscio chiuso molto stabile, mentre il sodio con Z = 11 presenta un elettrone esterno facilmente rimuovibile.
Quando osservi una serie di elementi con numero atomico crescente, noti andamenti regolari in queste grandezze. Tali andamenti spiegano perché alcuni elementi formano cationi con carica prevedibile, perché altri tendono a condividere elettroni e perché alcuni restano quasi inerti.
Il numero atomico diventa così un ponte concettuale tra equazioni quantistiche, come quelle del modello di Bohr e successivi, e fenomeni pratici, come il colore di un sale o la conducibilità di un metallo.
Uso del numero atomico nella tavola periodica
La moderna organizzazione degli elementi si basa proprio sul numero atomico, non più sulla sola massa. Ordinare per Z rivela pattern di comportamento chimico difficili da ignorare.
Nella tavola periodica, gli elementi seguono una sequenza crescente di Z, distribuendosi in periodi e gruppi con proprietà affini.
Questo criterio supera limiti storici della classificazione per massa, che produceva inversioni come quelle osservate per tellurio e iodio.
Grazie al numero atomico, ogni elemento trova una posizione coerente con la sua struttura elettronica. Di conseguenza, puoi prevedere con buona accuratezza acidità, basicità, tendenze di ossidazione e ruoli nelle reazioni redox.
Ecco i principali aspetti che ricavi subito da Z:
- Posizione nel periodo e quindi livello energetico più esterno
- Appartenenza al gruppo e somiglianze chimiche principali
- Tendenza a formare cationi o anioni stabili
- Probabile stato di ossidazione più comune
Quando impari a leggere la tavola attraverso il numero atomico, riduci lo sforzo mnemonico.
Ti basi infatti su regolarità strutturali, non su liste di eccezioni isolate. Questa prospettiva rende più intuitivo anche lo studio di blocchi specifici, come metalli di transizione e lantanidi.
Numero atomico tra storia della chimica e applicazioni
Lo sviluppo del concetto di numero atomico segna una svolta nella storia della teoria atomica. Non rappresenta soltanto un’etichetta ordinata, ma una grandezza fisica misurabile con precisione.
Dopo la proposta di Mendeleev basata principalmente sulla massa, esperimenti successivi mostrarono che la carica nucleare costituiva il parametro più fondamentale.
La scoperta dell’elettrone, del nucleo e dei protoni ha consolidato il ruolo centrale di Z.
Scienziati come Marie Curie evidenziarono, attraverso lo studio delle radiazioni, differenze tra isotopi che condividevano lo stesso numero atomico.
Oggi, tecniche come la spettroscopia X e la microscopia elettronica si fondano proprio su interazioni dipendenti da Z.
Sul piano applicativo, il numero atomico guida la scelta di materiali in medicina, elettronica e ingegneria dei materiali.
In radioterapia, per esempio, elementi con Z elevato interagiscono fortemente con la radiazione, permettendo trattamenti mirati.
In catalisi eterogenea, il numero atomico dei metalli di transizione influenza gli stati di ossidazione accessibili e quindi l’efficacia nelle trasformazioni chimiche.
Comprendere come Z entra in gioco in questi contesti ti aiuta a collegare nozioni teoriche e innovazioni tecnologiche contemporanee.
Una prospettiva unitaria sugli elementi chimici
Alla fine di questo percorso, il numero atomico emerge come principio organizzatore dell’intera chimica degli elementi.
Non è un semplice codice numerico, ma la traccia quantitativa della struttura del nucleo e, indirettamente, della distribuzione elettronica.
Vedere la tavola periodica come rappresentazione ordinata di Z permette di cogliere continuità e discontinuità nelle proprietà chimiche.
Le famiglie di elementi, le tendenze di ionizzazione, le affinità elettroniche e la formazione dei legami smettono di apparire come dati isolati. Diventano invece manifestazioni diverse di una stessa logica strutturale.
Il numero atomico collega così storia della scienza, tecniche sperimentali moderne e applicazioni tecnologiche che influenzano quotidianamente la società.
Ad esempio, la comprensione del comportamento dei metalli di transizione è fondamentale per sviluppare catalizzatori più efficienti, essenziali nell’industria chimica e nella produzione di energia pulita.
Inoltre, la manipolazione degli elementi nella tavola periodica ha portato alla scoperta di nuovi materiali, come i superconduttori, che promettono di rivoluzionare il trasporto elettrico.
Riuscire a leggere quella cifra con consapevolezza significa entrare in una grammatica profonda della materia, dove ogni elemento trova posto e significato in un disegno coerente e sorprendentemente elegante.