Ciclo di Krebs: il cuore della respirazione cellulare
Conoscere il ciclo di Krebs significa capire dove la cellula trasforma davvero il cibo in energia chimica utilizzabile.
Nel metabolismo aerobico, zuccheri, grassi e proteine convergono tutti in un passaggio cruciale: l’ingresso dell’acetil-CoA nel mitocondrio.
Qui entra in gioco il ciclo che ossida in modo fine il carbonio e libera elettroni ricchi di energia. Senza questo anello, la respirazione cellulare resterebbe incompleta e la resa di ATP crollerebbe in modo drastico. Per Medicina e Biologia, ciò significa spiegare perché un tessuto funziona, si ammala o resiste allo stress.
Questo processo non è solo una sequenza di reazioni.
È un nodo centrale in cui si intrecciano reazioni redox, sintesi di intermedi e controllo del bilancio energetico. Per questo il ciclo di Krebs è essenziale per interpretare analisi di laboratorio, farmacologia e fisiologia.
Nei prossimi paragrafi vedrai dove avviene, quali molecole produce, come dialoga con glicolisi e catena respiratoria, e perché è decisivo per organi ad alta richiesta energetica come cervello e cuore.
Struttura, sede e funzione generale del ciclo di Krebs
Il ciclo di Krebs avviene nella matrice del mitocondrio e rappresenta il centro operativo della respirazione aerobica.
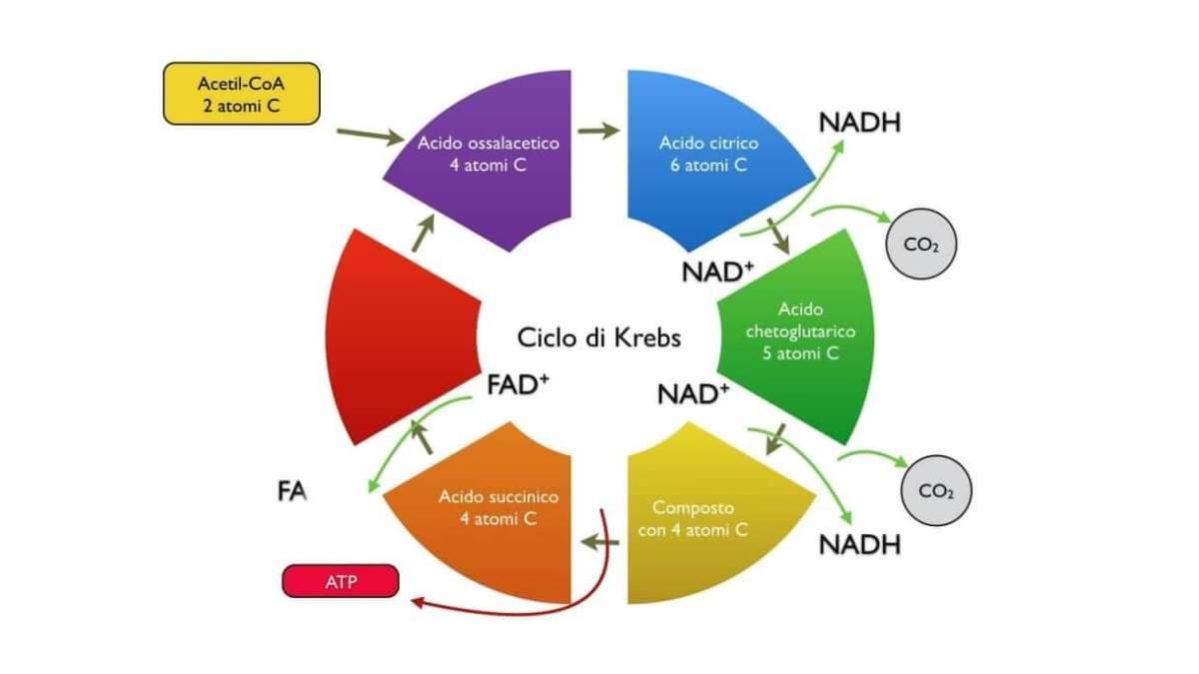
L’acetil-CoA, derivato da carboidrati, lipidi e aminoacidi, entra nel ciclo unendosi all’ossalacetato per formare citrato. Questo ciclo dell’acido citrico rigenera continuamente l’ossalacetato mentre ossida il carbonio ad anidride carbonica.
Il vero obiettivo, però, è trasferire elettroni ad accettori come NADH e FADH2, che alimenteranno poi la catena respiratoria. Ogni giro produce anche una molecola di GTP o ATP, utile ma quantitativamente minore rispetto all’energia che arriverà dopo.
Se stai ripassando, immagina il ciclo di Krebs come una ruota.
Ogni giro, a partire da un acetil-CoA, fornisce tre NADH, un FADH2 e una molecola ad alta energia. In un muscolo in attività intensa, migliaia di queste ruote girano in parallelo. Il risultato è un flusso continuo di equivalenti riducenti verso la fosforilazione ossidativa, che sostiene la contrazione prolungata.
Questa organizzazione ciclica consente un controllo fine. Piccole variazioni di substrati, come l’ossalacetato, o di cofattori, modulano in tempo reale la velocità del ciclo, adattando la produzione energetica alle esigenze istantanee della cellula.
Connessioni con glicolisi, catena respiratoria e bilancio energetico
Il ciclo di Krebs non lavora mai isolato: dialoga costantemente con glicolisi e catena di trasporto degli elettroni.
La glicolisi fornisce piruvato, che viene decarbossilato a acetil-CoA dal complesso della piruvato deidrogenasi.
Da lì l’acetil-CoA entra nel ciclo. Gli equivalenti riducenti prodotti, come NADH, raggiungono la catena respiratoria, dove generano grandi quantità di ATP.
In questo modo, le rese energetiche delle singole vie si sommano. Per chi studia Medicina, questo legame spiega perché un difetto mitocondriale abbatte la produzione di energia anche se la glicolisi funziona.
Ecco le fasi chiave che devi ricordare:
- Formazione del citrato da acetil-CoA e ossalacetato
- Decarbossilazioni che producono CO2 e NADH
- Ossidazione del succinato con formazione di FADH2
- Rigenerazione dell’ossalacetato pronto per un nuovo giro
Dal punto di vista del bilancio energetico, il ciclo di Krebs costituisce un moltiplicatore.
Un singolo glucosio, attraverso glicolisi, ciclo e fosforilazione ossidativa, può portare a decine di molecole di ATP. Per questo, negli studi su dimagrimento e metabolismo basale, si considera sempre l’efficienza della respirazione cellulare, e non solo le calorie introdotte con la dieta.
Rilevanza clinica: dal paracetamolo ai deficit vitaminici
Perché il ciclo di Krebs è così importante in Medicina?
Perché molte condizioni cliniche ne alterano i flussi.
L’intossicazione da paracetamolo è un esempio efficace.
Quando le riserve di glutatione epatico crollano, aumentano radicali liberi che danneggiano il mitocondrio.
Il risultato è un blocco del ciclo di Krebs, con drastica riduzione di ATP e morte cellulare. Lo stesso accade in alcune ischemie: senza ossigeno, la catena respiratoria si ferma e il ciclo rallenta fino quasi a spegnersi.
Anche le carenze di cofattori colpiscono il ciclo. Il deficit di vitamina B1, essenziale per la piruvato deidrogenasi, riduce la formazione di acetil-CoA.
Il magnesio è richiesto per vari enzimi mitocondriali. In un paziente con malnutrizione grave, questi deficit si traducono in affaticabilità, intolleranza allo sforzo e, nei casi peggiori, danno neurologico.
Non è “stanchezza generica”, ma conseguenza biochimica precisa.
Comprendere queste relazioni permette di leggere meglio enzimi sierici, lattato e alterazioni acido-base.
In terapia intensiva, per esempio, l’osservazione del lattato elevato richiama subito una riduzione globale del flusso attraverso il ciclo di Krebs e la fosforilazione ossidativa.
Ruolo nella cellula eucariote, nei tessuti e nei diversi organismi
In ogni cellula eucariote, il ciclo di Krebs rappresenta il collegamento tra catabolismo e biosintesi, non solo una “centrale elettrica”.
Nel fegato, molti intermedi vengono sottratti al ciclo per sintetizzare aminoacidi, emoglobina o corpi chetonici.
Nel tessuto adiposo, il citrato esportato dal mitocondrio alimenta la lipogenesi.
Nei neuroni, invece, la priorità resta la produzione stabile di ATP. Questo spiega perché il cervello risulta vulnerabile a difetti mitocondriali.
In Biologia, studiare queste differenze tra tessuti aiuta a capire fenomeni come la termogenesi o l’adattamento al digiuno prolungato.
Nei batteri aerobici, che non hanno mitocondri, le stesse reazioni avvengono nel citoplasma o sulla membrana.
Alcuni microrganismi usano vie affini, come il ciclo di Krebs incompleto o il ciclo del gliossilato, per sopravvivere in condizioni particolari.
Anche nelle piante, i mitocondri collaborano con i cloroplasti: di giorno sfruttano i substrati della fotosintesi, di notte mantengono in funzione le cellule consumando riserve.
Questa versatilità rende il ciclo di Krebs un modello perfetto per studiare l’evoluzione dei metabolismi e i diversi stili di vita cellulare, dai lieviti alle cellule umane.
Strategie di studio efficaci per memorizzare il ciclo di Krebs
Memorizzare ogni passaggio del ciclo di Krebs può sembrare frustrante, ma esistono strategie più razionali della semplice ripetizione.
Un primo passo è costruire uno schema chiaro, sempre nello stesso ordine.
Parti dai reagenti che conosci già, come acetil-CoA e ossalacetato, poi aggiungi via via intermedi e cofattori.
Usa colori diversi per reazioni redox, decarbossilazioni e passaggi che producono GTP o ATP. Questa codifica visiva riduce il carico della memoria a breve termine.
Efficaci anche piccole mnemotecniche.
Per esempio, collega mentalmente ogni enzima all’azione che compie e non solo al nome.
Quando ripassi, cerca di spiegare ad alta voce il percorso, come se stessi preparando un esame di Biochimica. Questo tipo di richiamo attivo rafforza i collegamenti logici, non solo la sequenza mnemonica.
Infine, collega sempre il ciclo di Krebs a contesti clinici o fisiologici concreti, come l’esercizio intenso o il digiuno.
In questo modo il percorso non resta un elenco astratto di molecole, ma diventa un racconto coerente di come la cellula produce energia e mantiene stabile il proprio ambiente interno.
Perché il ciclo di Krebs resta un tema cardine per le scienze della vita
Vedere il ciclo di Krebs solo come una “lista da imparare” significa perdere la sua vera potenza esplicativa.
Questo circuito racchiude in poche reazioni la logica del metabolismo energetico: ingresso dei substrati, utilizzo mirato degli elettroni, produzione di ATP, rifornimento di intermedi biosintetici.
Per questo entra in ogni discussione su fisiologia, patologia, farmacologia e persino nutrizione.
Quando un farmaco danneggia il mitocondrio, quando una mutazione colpisce un enzima, quando l’omeostasi energetica salta, il ciclo di Krebs è quasi sempre coinvolto.
Nel tempo, le tecniche di imaging e biologia molecolare stanno mostrando il ciclo in azione, dentro tessuti e singole cellule.
Questo trasforma uno schema statico in un processo dinamico, regolato istante per istante.
Ad esempio, l’uso della spettroscopia di risonanza magnetica nucleare consente di visualizzare i cambiamenti metabolici in tempo reale.
Chi studia Medicina o Biologia non trova qui solo materia d’esame, ma una chiave interpretativa per la clinica, la ricerca e la comprensione profonda della vita cellulare. Ed è per questo che questo ciclo continua a occupare un posto centrale nei manuali e nei laboratori, influenzando anche lo sviluppo di terapie mirate nelle malattie metaboliche.